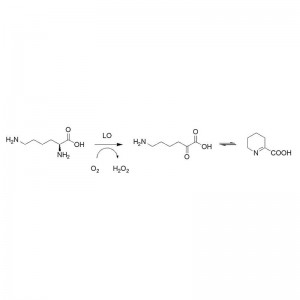
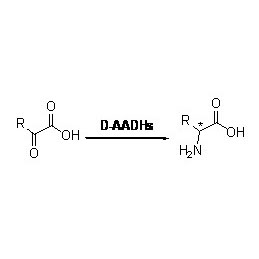
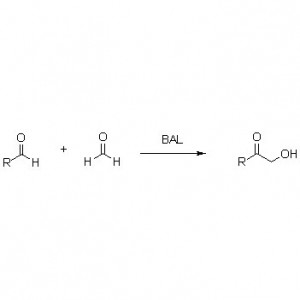
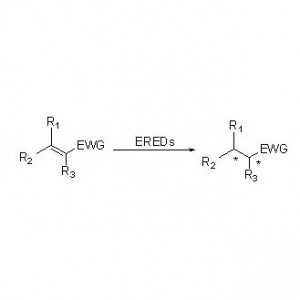
Transaminase (ATA)
Enzimas: Son catalizadores biolóxicos macromoleculares, a maioría das encimas son proteínas.
Transaminases: Unha clase de encimas que catalizan a transferencia de aminoácidos entre aminoácidos e cetoácidos. As transaminases son encimas biolóxicos clave na síntese asimétrica e na resolución racémica de aminas quirais.
As aminotransferases pódense dividir en catro clases segundo a súa secuencia e estrutura: Ⅰ, Ⅱ, Ⅲ e Ⅳ. As ω-aminotransferases pertencen ás transaminases de clase II e úsanse habitualmente na preparación de aminas quirais e aminoácidos non naturais, como os β-aminoácidos.
ω-aminotransferases: Na maioría dos casos, a ω-transaminase refírese a unha clase de encimas que realizan reaccións catalíticas de transferencia de amoníaco sen α-aminoácido como substrato ou produto.
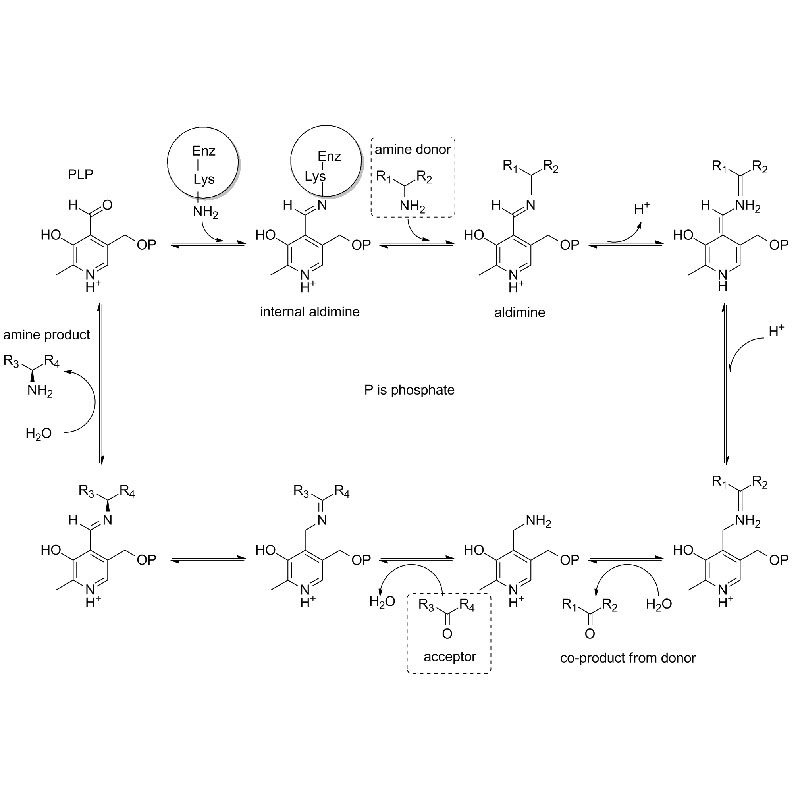
Mecanismo catalítico:
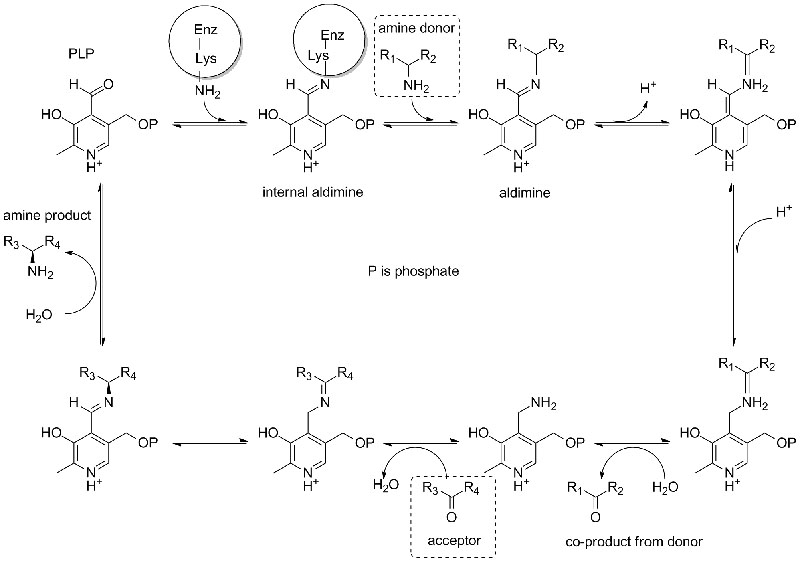
| Enzimas | Código do produto | Código do produto |
| Enzima en po | ES-ATA-101~ ES-ATA-165 | un conxunto de 65 ω-transaminases, 50 mg cada unha 65 unidades * 50 mg/unidade, ou outra cantidade |
| Kit de cribado (SynKit) | ES-ATA-6500 | un conxunto de 65 ω-transaminases, 1 mg cada unha 65 elementos * 1 mg / elemento |
★ Alta especificidade do substrato.
★ Forte selectividade quiral.
★ Alta eficiencia de conversión.
★ Menos subprodutos.
★ Condicións de reacción suaves.
★ Respectuoso co medio ambiente.
➢ A selección de encimas debe levarse a cabo para substratos específicos debido á especificidade do substrato e obter un encima que catalice o substrato diana co mellor efecto catalítico.
➢ Nunca o poña en contacto con condicións extremas como: altas temperaturas, pH alto/baixo e solventes orgánicos con alta concentración.
➢ Normalmente, o sistema de reacción debe incluír substrato, solución tampón, doante de aminoácidos (como aminoácidos e 1-feniletilamina) ou receptor (como cetoácidos), coenzima (PLP) e cosolvente (como DMSO).
➢ O ATA debe engadirse por último ao sistema de reacción, despois de axustar o pH e a temperatura ás condicións de reacción.
➢ Todos os tipos de ATA teñen diversas condicións óptimas de reacción, polo que cada un deles debería ser estudado individualmente.
Exemplo 1 (síntese de sitagliptina, síntese asimétrica)(1):
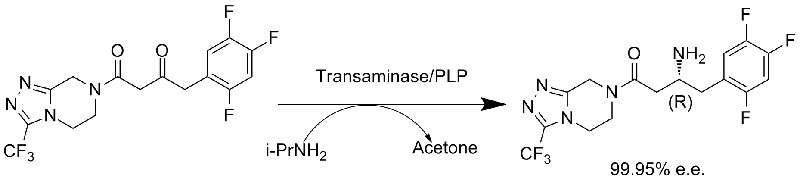
Exemplo 2 (Mexiletina, combinación de resolución cinética con síntese asimétrica)(2):
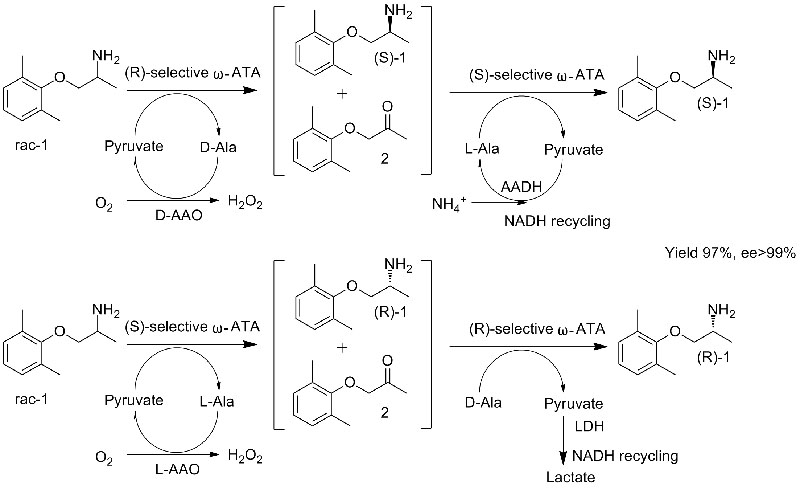
1 Savile CK, Janey JM, Mundorff EC e outros. Science, 2010, 329(16), 305-309.
2 Koszelewski D, Pressnitz D, Clay D, et al. Cartas orgánicas, 2009,11(21):4810-4812.